Johnson & Johnson detiene ensayos de vacuna contra COVID-19 por participante enfermo
J&J es el décimo laboratorio a nivel global que realiza pruebas en fase 3 contra el coronavirus, y el cuarto en Estados Unidos
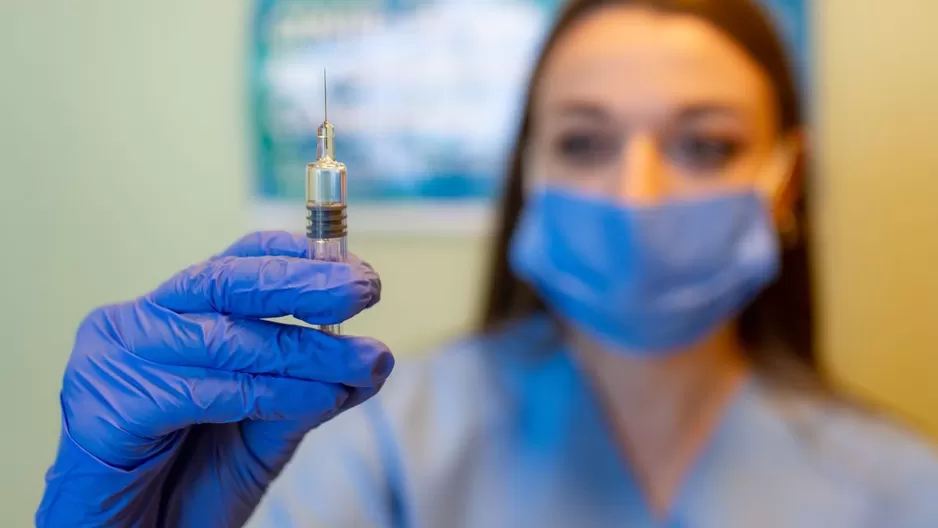
La farmacéutica estadounidense Johnson & Johnson señaló que detuvo temporalmente la prueba clínica de su vacuna contra COVID-19 debido a que uno de sus participantes se enfermó.
"Hemos detenido temporalmente la administración de nuevas dosis en todos nuestros ensayos clínicos de la vacuna contra covid-19, incluido el ensayo de fase 3 ENSEMBLE, debido a una enfermedad inexplicable en un participante del estudio", dijo la compañía en un comunicado.
La pausa significa que el sistema de inscripción en línea fue cerrado para el ensayo clínico de 60 mil pacientes, mientras se convoca al comité independiente de seguridad del paciente.
J&J sostuvo que los efectos adversos serios eran "una parte esperada de cualquier estudio clínico, especialmente uno grande". Según los lineamientos de la compañía, pueden detener un estudio para determinar si el efecto adverso se debió a la droga en cuestión y si se puede retomar el estudio.
La fase 3 del estudio de Johnson & Johnson empezó a reclutar voluntarios a finales de septiembre, con la meta de inscribir hasta 60 mil participantes en más de 200 localidades en Estados Unidos y el mundo.
Los otros países donde se realizaban las pruebas son Argentina, Brasil, Chile, Colombia, México, Perú y Sudáfrica.
J&J es el décimo laboratorio a nivel global que realiza pruebas en fase 3 contra la COVID-19, y el cuarto en Estados Unidos.
La compañía recibió $1.450 millones del gobierno estadounidense, en el marco de una iniciativa para el desarrollo de una vacuna contra el virus que ha matado a casi 215 mil personas en el país.
La vacuna está basada en una sola dosis de un adenovirus que causa la gripe, modificado para que no se replique, ello combinado con una parte del nuevo coronavirus que usa para invadir las células humanas.
J&J usó la misma tecnología para su vacuna contra el ébola que fue aprobada para su mercadeo por la Comisión Europea en julio.
Pruebas en monos que fueron publicadas en la revista Nature mostraron que la vacuna otorgaba una protección completa o casi completa contra una infección del virus en los pulmones y la nariz.
AFP